Qui sommes-nous ?
Le microbiote intestinal est un nouvel acteur dans la santé et ses altérations sont impliquées dans de nombreuses maladies. Il apparaît donc logique de cibler le microbiote intestinal d’un point de vue thérapeutique.
Dans ce contexte, la transplantation de microbiote fécal (TMF) a émergé comme une nouvelle option thérapeutique. L’expertise combinée de plusieurs équipes de l’AP HP (Hôpital Saint Antoine et Pitié Salpetrière) a permis de donner naissance au centre de transplantation fécale de l’AP-HP qui accueille et prend en charge les patients ayant des infections à Clostridioides difficile, et les volontaires sains qui souhaitent contribuer aux soins en devenant donneurs de selles.
A ce jour, la TMF n’est applicable en routine clinique que dans les infections récidivantes à Clostridioides difficile avec 80-90% de succès.
L’activité du centre s’étend sur l’ensemble des hôpitaux de l’Ile de France (AP-HP et hors AP-HP)
Elle s’articule autour de l’étroite collaboration du coordinateur du centre, de gastro-entérologues, d’infectiologues, de pharmaciens et des laboratoires de biologies hospitaliers.
Le centre travaille en étroite collaboration avec le Groupe Français de Transplantation fécale (www.gftf.fr) regroupant les différents experts français de la TMF.
Nos objectifs
Le centre a pour mission de produire et coordonner l’administration des transplants de microbiote fécal dans le cadre du soin (infections récidivantes à Clostridioides . difficile).
Pour cela, le centre coordonne et réalise le recrutement de donneurs volontaires sains sur la base de critères cliniques et biologiques strictes permettant d’éliminer le risque de transmission de pathogènes connus selon les recommandations de l’ANSM.
– Les experts du centre, fort d’une expertise pluri-disciplinaire complémentaire, conseillent et valident les indications de TMF afin de garantir le bon usage de cette thérapeutique et la sécurité de la transplantation fécale.
e-learning
Le centre de transplantation de l’AP-HP a également pour mission de favoriser la diffusion des connaissances autour du microbiote intestinal et de la transplantation fécale ainsi que de promouvoir la recherche. Une chaîne Youtube a été ainsi créée abordant les différentes notions sur le rationnel, les indications et les modalités pratiques de réalisation de la TMF en 2022.
Chaîne Youtube Centre de TMF de l’AP-HP
https://www.youtube.com/channel/UC2l9AbsuNpR5dKjnIJG_ZUw
CV à consulter
Coordinateur
Pr Harry Sokol
 Harry Sokol, coordinateur du centre de transplantation fécale de l’AP-HP, est professeur dans le département de Gastroentérologie de l’hôpital Saint-Antoine (APHP, Paris, France), co-directeur de l’équipe « Microbiote, Intestin et inflammation » (INSERM CRSA), chef du groupe Imipath (INRAe, MICALIS) et coordinateur de la FHU PaCeMM (« Paris Center for Microbiome Medicine »).
Harry Sokol, coordinateur du centre de transplantation fécale de l’AP-HP, est professeur dans le département de Gastroentérologie de l’hôpital Saint-Antoine (APHP, Paris, France), co-directeur de l’équipe « Microbiote, Intestin et inflammation » (INSERM CRSA), chef du groupe Imipath (INRAe, MICALIS) et coordinateur de la FHU PaCeMM (« Paris Center for Microbiome Medicine »).
Expert internationalement reconnu dans les domaines des maladies inflammatoires chroniques de l’intestin (MICI) et du microbiote intestinal, il a publié plus de 240 articles sur ces sujets. Son travail sur le rôle du microbiote intestinal dans la pathogenèse des MICI a abouti à des articles marquants décrivant les anomalies du microbiote associée aux MICI et le rôle de la bactérie commensale Faecalibacterium prausnitzii essentielle dans l’homéostasie intestinale et dans les MICI. Actuellement, son travail se concentre sur le déchiffrement des interactions microbiote intestinal-hôte dans la santé et les maladies afin de mieux comprendre leur pathogenèse et développer des traitements innovants. A côté de la recherche fondamentale, il participe également à la recherche translationnelle, est président du Groupe Français de Transplantation Fécale, et coordonne plusieurs essais contrôlés randomisés évaluant la transplantation de microbiote fécale dans la maladie de Crohn et la rectocolite hémorragique.
Médecins temps pleins
Dr Alexandre Bleibtreu
Alexandre Bleibtreu, membre du centre de transplantation fécale de l’AP-HP, est praticien hospitalier dans le service de Maladies Infectieuses et Tropicales et référent anti-infectieux de l’hôpital Pitié Salpêtrière (APHP, Paris, France). Titulaire d’une thèse de science en microbiologie fondamentale, il est membre de l’équipe « Emergence and diffusion of multiple resistance against antibiotics » du Pr Alexandra Aubry, au Centre d’Immunologie et des Maladies Infectieuses (Cimi-Paris), INSERM U1135. Il est membre de la FHU PaCeMM (« Paris Center for Microbiome Medicine »). Il a participé à la création de l’APHP-FMT center et y apporte son expertise d’infectiologue. Il coordonne la commission consultative des indications compassionnelles du Groupe Français de Transplantation Fécale (GFTF), il participe à plusieurs projets de recherche autour du microbiote. Spécialiste en thérapeutiques anti-bactériennes allant de l’antibiothérapie (bon usage des anti-infectieux, nouvelles molécules antibiotiques) aux stratégies innovantes non antibiotiques (transplantation fécale, phagothérapie) son intérêt se porte sur la possibilité d’apporter des solutions thérapeutiques efficaces pour guérir les patients tout en respectant au maximum l’environnement que représente les microbiotes humains et environnementaux.
Dr Cécilia Landman
Cécilia Landman, médecin dans le service de Gastroentérologie et Nutrition à l’hôpital Saint Antoine, a complété sa formation médicale par un parcours de recherche sur la thématique du microbiote intestinal dans les maladies inflammatoires chroniques intestinales (MICI). Elle est également titulaire du DESC de cancérologie. Elle participe également à l’activité d’éducation thérapeutique dans les MICI. Elle est aussi très impliquée dans l’activité de transplantation de microbiote fécal pour les infections récidivantes à Clostridioides difficile récidivant et dans le cadre de la recherche clinique chez les patients atteints de MICI.
Dr Paul Mclellan
Paul Mclellan, médecin dans le service de Gastroentérologie et Nutrition à l’hôpital Saint Antoine, et aussi titulaire d’un Master de recherche orienté vers les modifications du microbiote intestinale dans les maladies inflammatoires intestinales (MICI). Il est impliqué dans les essais thérapeutique concernant la transplantation de microbiote fécal (TMF) chez les patients atteints de MICI, la transplantation de microbiote fécal pour les infections récidivantes à Clostridioides difficile et la sélection des donneurs de selles. Il s’occupe par ailleurs des patients atteints de MICI en proposant une prise en charge globale et intégrative.
Pharmacie
Dr Anne Christine Joly
 Anne-Christine Joly est pharmacien responsable pharmacotechnie : UPAC&C (Unité de Préparation des AntiCancéreux et Contrôle) et UPTM (Unité de Préparation de Transplants de Microbiote, créée en 2015) à l’Hôpital Saint Antoine – Groupe Hospitalier AP-HP.Sorbonne Université. Membre du Groupe Français de Transplantation Fécale depuis sa création en 2014 et de la FHU PaCeMM (« Paris Center for Microbiome Medicine »), elle participe activement à l’activité de préparation des transplants pour le soin et dans la mise en œuvre des essais cliniques multicentriques nécessitant la préparation de transplants de microbiote sous différentes formes pharmaceutiques.
Anne-Christine Joly est pharmacien responsable pharmacotechnie : UPAC&C (Unité de Préparation des AntiCancéreux et Contrôle) et UPTM (Unité de Préparation de Transplants de Microbiote, créée en 2015) à l’Hôpital Saint Antoine – Groupe Hospitalier AP-HP.Sorbonne Université. Membre du Groupe Français de Transplantation Fécale depuis sa création en 2014 et de la FHU PaCeMM (« Paris Center for Microbiome Medicine »), elle participe activement à l’activité de préparation des transplants pour le soin et dans la mise en œuvre des essais cliniques multicentriques nécessitant la préparation de transplants de microbiote sous différentes formes pharmaceutiques.
Pr Nathalie Kapel
Nathalie Kapel est biologiste médical. Elle dirige le laboratoire de Coprologie Fonctionnelle (APHP.6 Sorbonne Université) qui est labellisé comme laboratoire de référence pour l’exploration de l’homéostasie intestinale par la mesure des nutriments et des métabolites dans les selles. Elle a une longue expérience de la transplantation fécale puisqu’elle collabore avec le clinicien pour effectuer cette procédure dès 2012 et était responsable de la supervision de la préparation des transplantations fécales dans le premier essai randomisé européen qui a évalué l’efficacité de la transplantation fécale chez les patients atteints de multi-drogue- bactéries résistantes. Elle est membre de l’unité INSERM S_1139 où elle a dirigé l’axe de recherche sur la transplantation du microbiote fécal qui évalue l’efficacité des produits du microbiote dans diverses conditions expérimentales dans des modèles précliniques. En collaboration avec l’INRAE, l’Université de Paris et l’APHP, elle a développé un brevet pour un procédé de lyophilisation d’échantillon fécal
Dr Rachel Sintes
 Rachel SINTES est pharmacienne assistant spécialiste de l’unité de préparation des transplants de microbiote (UPTM) au sein de l’hôpital Saint-Antoine. Spécialisée en pharmacotechnie, elle a, durant son internat, participé à une étude sur le développement d’une formulation sèche à base de microbiote fécal, à l’origine de sa thèse de fin d’étude. Son travail consiste en l’organisation du circuit des dons et des préparations à base de microbiote fécal dans le domaine du soin et de la recherche clinique. Avec l’équipe de l’UPTM, ils participent également au développement de l’activité en France et à l’amélioration de la pratique dans le domaine de la pharmacotechnie.
Rachel SINTES est pharmacienne assistant spécialiste de l’unité de préparation des transplants de microbiote (UPTM) au sein de l’hôpital Saint-Antoine. Spécialisée en pharmacotechnie, elle a, durant son internat, participé à une étude sur le développement d’une formulation sèche à base de microbiote fécal, à l’origine de sa thèse de fin d’étude. Son travail consiste en l’organisation du circuit des dons et des préparations à base de microbiote fécal dans le domaine du soin et de la recherche clinique. Avec l’équipe de l’UPTM, ils participent également au développement de l’activité en France et à l’amélioration de la pratique dans le domaine de la pharmacotechnie.
Dr Gabriele Navelli
 Gabriele Navelli, pharmacien italien, a complété ses études dans la faculté de pharmacie de Paris (Université de Paris). Après une période à l’Hôpital Cochin dans l’UPSO2 (Unité des préparations stériles ophtalmologiques et oncologiques), il travaille aujourd’hui en tant qu’ingénieur de recherche hospitalier dans le service de l’UPTM (Unité de préparation des transplants de microbiote) à l’Hôpital Saint Antoine. Il participe à la préparation en équipe et au contrôle des éléments thérapeutiques conformément aux protocoles et aux bonnes pratiques. Il collabore avec les différents PUI des centres demandeurs des transplants pour mettre en place le système de sous-traitance. Il est également impliqué dans le cadre de la recherche clinique chez les patients atteints de MICI.
Gabriele Navelli, pharmacien italien, a complété ses études dans la faculté de pharmacie de Paris (Université de Paris). Après une période à l’Hôpital Cochin dans l’UPSO2 (Unité des préparations stériles ophtalmologiques et oncologiques), il travaille aujourd’hui en tant qu’ingénieur de recherche hospitalier dans le service de l’UPTM (Unité de préparation des transplants de microbiote) à l’Hôpital Saint Antoine. Il participe à la préparation en équipe et au contrôle des éléments thérapeutiques conformément aux protocoles et aux bonnes pratiques. Il collabore avec les différents PUI des centres demandeurs des transplants pour mettre en place le système de sous-traitance. Il est également impliqué dans le cadre de la recherche clinique chez les patients atteints de MICI.
Sandrine Delage
Sandrine Delage est diplômée préparatrice en pharmacie Hospitalière.
Actuellement, préparatrice référente de l’Unité de Préparation de Transplantation Microbiote (UPTM) de l’hôpital Saint-Antoine (APHP, Paris, France), elle a intégré cette activité depuis sa mise en place.
Elle a travaillé plusieurs années dans l’Unité de Préparation des Anticancéreux et Contrôle (UPAC&C) de l’hôpital Saint Antoine dont elle est devenue référente de la formation des préparateurs à la manipulation des préparations cytotoxiques. Elle a également été référente du laboratoire de contrôle.
Elle a obtenu le Diplôme Universitaire « Analyse et Gestion des Risques en Santé » à l’Université Paris Descartes dont le mémoire portait sur une étude de risques sur les différents contrôles de préparations cytotoxiques au sein de l’UPAC.
Laboratoire
Bactériologie
Pr Frédéric Barbut
Frédéric Barbut est un microbiologiste médical avec une vaste expérience dans le contrôle des infections, les infections nosocomiales et l’épidémiologie. Depuis 1994, il travaille sur différents agents responsables d’infections nosocomiales dont les bactéries multirésistantes, Clostridioides difficile et Legionella. En tant que responsable du Laboratoire national de référence pour Clostridioides difficile en 2006, son objectif était d’améliorer les stratégies de diagnostic, de développer des marqueurs épidémiologiques moléculaires et de définir le fardeau de la maladie en France/Europe en termes de morbi-mortalité et de coûts. Il a initié plusieurs projets concernant i) l’incidence de Clostridioides difficile dans différentes populations et dans la communauté, ii) la phylogénie de Clostridioides difficile, iii) l’analyse des facteurs de virulence de Clostridioides difficile par des approches génomiques et transcriptomiques, et iv) la relation entre Clostridioides difficile et le microbiote intestinal analysée par métagénomique 16S. En 2018, il est devenu directeur adjoint de l’unité INSERM S-1139 intitulée « Physiopathologie et pharmacotoxicologie du placenta humain – Microbiote pré- et post-natal ». Il a développé des projets sur le microbiome placentaire et commencé à étudier le microbiote intestinal des prématurés à travers différentes cohortes (PREMAFLORA, CLOSNEC, EPIFLORE). Son groupe a identifié des candidats probiotiques actuellement à l’étude dans des modèles animaux pour prévenir l’entérocolite nécrosante, l’infection à Clostridioides difficile, la colonisation par des bactéries multirésistantes ou la prévention des allergies alimentaires. Son groupe a également initié un projet de recherche sur la classification des donneurs de selles ou la transplantation de microbiote fécal en utilisant des approches génomiques, métabolomiques et immunologiques.
Dr Catherine Eckert
Catherine Eckert, Maitre de Conférences des Universités-Praticien Hospitalier, biologiste dans le département de bactériologie de l’hôpital Saint-Antoine, AP-HP.Sorbonne-Université, Paris, France.
Responsable médicale du diagnostic des infections à Clostridioides difficile au sein du département de bactériologie situé à l’hôpital Saint-Antoine et collaboratrice du Centre National de Référence Clostridioides difficile.
Recherche clinique et expertise de techniques diagnostic dans le domaine des infections à Clostridioides difficile.
Recherche translationnelle au sein de l’équipe EDIRA (Emergence et propagation des multi-résistances aux Antibiotiques), Centre d’Immunologie et de Maladies Infectieuses (Cimi), Sorbonne-Université, Paris. Ses travaux de recherche sont centrés sur les nouvelles stratégies de lutte contre l’antibiorésistance. Ils portent en particulier sur l’utilisation des bactériophages comme stratégie de décolonisation du tube digestif des patients porteurs de Klebsiella pneumoniae Multi-Résistantes. La décolonisation du portage digestif des Bactéries Multi-Résistantes et Bactéries Hautement Résistantes émergentes dans les flores commensales est considérée comme une priorité par l’OMS pour lutter contre la dissémination et les conséquences de l’antibiorésistance.
Dr Imane Mostaghat
Imane Mostaghat, Assistante Hospitalo-Universitaire (AHU), microbiologiste à l’Hôpital Saint-Antoine AP-HP.
Elle exerce ses activités hospitalières au sein du service de microbiologie de l’environnement et de bactériologie générale, où elle est en charge de la bactériologie pédiatrique et du diagnostic des infections gastro-intestinales.
Elle mène ses activités de recherche au sein de l’UMR INSERM S-1139 « Fonctions placentaires et reproductives, microbiote pré- et post-natal (FPRM) » à la Faculté de Pharmacie de Paris.
Elle participe également à des projets menés au sein du Laboratoire national de référence Clostridioides difficile, consacrés à l’expertise et à l’évaluation de nouvelles techniques diagnostiques innovantes.
Virologie
Pr Laurence Morand-Joubert
Laurence Morand-Joubert est médecin, professeur des Universités-Praticien hospitalier, responsable du département de Virologie (rive droite) comprenant les 3 services de virologie de Saint-Antoine, Trousseau et Tenon. Elle appartient à la structure de recherche labellisée : TheraVir « Therapeutic strategies for HIV infection and associated viral diseases », de l’Institut Pierre Louis d’Epidémiologie et de Santé Publique, INSERM UPMC UMRS_S 1136, labellisée par l’INSERM et Sorbonne Université, classée A par l’AERES.
Depuis de nombreuses années, sa recherche est centrée sur le VIH avec 3 thèmes principaux que sont le réservoir viral, la résistance du VIH aux antirétroviraux et l’étude de la transmission de l’infection. Dans ce cadre, elle a été l’investigatrice principale de plusieurs essais thérapeutiques de l’ANRS comme Trianon (081), Narval (088), Alizé (099). Actuellement, elle est responsable des analyses virologiques sur le réservoir et la résistance du VIH dans 2 essais nationaux d’intermittence thérapeutique, promus par l’ANRS-MIE (Quatuor et Duetto).
D’autre part, elle et son équipe sont très impliquées dans l’activité et la recherche clinique concernant la virologie périnatale et pédiatrique orientée sur les infections respiratoires, les infections infantiles comme la rougeole, l’infection à parvovirus et aussi les gastro-entérites virales.
Dr Aurélie Schnuriger
Aurélie Schnuriger, Maître de Conférences des Universités – Praticien Hospitalier, Centre de Recherche Saint-Antoine UMR_S 938, groupe « Carcinome hépatocellulaire, Virus de l’hépatite B et réponse immunitaire », Faculté de Médecine, Sorbonne Université, Paris, et Département de virologie groupe hospitalier APHP.Sorbonne Université, site Trousseau.AP-HP . Responsable pratique de l’unité de virologie du site Trousseau, qui sera prochainement regroupée sur le site de Saint-Antoine, sous la direction du Pr Laurence Morand-Joubert. L’activité de diagnostic de notre unité est essentiellement dirigée vers l’identification et le suivi des viroses respiratoires (dont SARS-CoV-2), méningées, entériques et materno-fœtales, pour les patients des hôpitaux St Antoine, Tenon et Trousseau. Nous réalisons la recherche de virus dans les selles pour les virus à transmission entérique (enterovirus, parechovirus) et pour les virus à transmission et tropisme entérique et responsables de manifestations cliniques de gastroentérite (rotavirus, adénovirus, norovirus), par des techniques de biologie moléculaire (PCR) ciblées ou multiplex
Parasitologie
Pr Christophe Hennequin
Christophe Hennequin est Professeur des Universités-Praticien-Hospitalier au sein du groupe Sorbonne Université. Il est chef du service de Parasitologie-Mycologie de l’hôpital Saint-Antoine à Paris. Ses travaux de recherche clinique portent sur l’optimisation et l’évaluation de techniques diagnostiques principalement en mycologie médicale. Il dirige des recherches plus expérimentales au sein du Centre de Recherche Saint-Antoine. Elles ont pour but de mieux comprendre les interactions entre l’épithélium bronchique et le pathogène environnemental, Aspergillus fumigatus. Il enseigne au sein de la faculté de Médecine de Sorbonne Université ainsi qu’en licence et master, proposés par la Faculté des Sciences et de l’Ingénierie de la même Université. Il est Président de l’InterCollégiale de Biologie Médicale de l’Assistance Publique-Hôpitaux de Paris et Rédacteur en Chef du Journal of Medical Mycology.
Dr Alicia Moreno Sabater
Alicia Moreno Sabater est Maître de conférences – Praticien Hospitalier au sein du service de Parasitologie-Mycologie de l’hôpital Saint-Antoine (APHP, Paris, France). Son travail de recherche a été initialement dédié à la mise au point de modèles de souris humanisées pour l’études du paludisme à Plasmodium falciparum. Depuis son intégration comme MCU-PH, son travail s’est orienté à l’étude de l’immunité humorale systémique et le mycobiote intestinal. Son travail a permis de montrer une corrélation significative entre la diversité du mycobiote intestinal et la diversité de la réponse humorale systémique. Actuellement, ses recherches se concentrent sur le déchiffrement des interactions des écosystèmes fongiques-bactériens et leurs impacts dans l’axe intestin-foie. A côté de la recherche fondamentale, elle participe également à la recherche clinique sur les dermatomycoses et la résistance aux antifongiques.
Infirmière de coordination
Sandrine Truong
 Coordinatrice du centre de transplantation fécale de l’AP-HP, elle a été infirmière dans le service de chirurgie digestive pendant 8 ans puis dans le service de gastro entérologie et nutrition de l’hôpital Saint Antoine pendant 2 ans.
Coordinatrice du centre de transplantation fécale de l’AP-HP, elle a été infirmière dans le service de chirurgie digestive pendant 8 ans puis dans le service de gastro entérologie et nutrition de l’hôpital Saint Antoine pendant 2 ans.
Au cours de son expérience au sein du service de gastro entérologie, elle a pu participer à la sélection des donneurs volontaires au don de selles pour le soin des infections récidivantes à Clostridioides difficile par transplantation de microbiote fécale.
Le rôle de la coordinatrice de transplantation de microbiote fécal (TMF) est d’organiser les TMF au sein ou hors de l’hôpital Saint Antoine, majoritairement pour des infections à Clostridioides difficile récidivantes. Elle travaille en étroite collaboration avec les médecins du centre de TMF et l’équipe de l’unité de préparation en pharmacie. Elle est l’interlocutrice principale des médecins demandeurs et du patient receveur. Elle les informe et guide sur les différentes étapes d’organisation de la TMF mais aussi pendant et après la TMF (procédures d’administration, surveillance post TMF…). Par ailleurs, elle joue aussi un rôle important dans le recrutement des donneurs de selles (volontaires sains) et dans leur validation (analyse de sang et de selles). Elle organise la collecte et la livraison des dons en pharmacie. Elle est joignable de l’extérieur par les médecins demandeurs pour avis et validation d’une indication de TMF par les médecins du centre de transplantation fécale de l’APHP.
Le microbiote intestinal est composé de l’ensemble des micro-organismes vivant au sein du tractus digestif. Il regroupe plusieurs règnes du vivant : bactéries, parasites, archées, champignons et virus. Chez l’Homme, il est composé d’environ 1013 micro-organismes, principalement des bactéries, avec une répartition suivant un gradient de concentration progressivement croissant le long du tube digestif, avec une concentration maximale au niveau du rectum. Depuis 20 ans, son étude a connu une révolution conceptuelle et technologique avec l’avènement des outils de biologie moléculaire qui ont permis la découverte et l’étude d’espèces, principalement des bactéries, non cultivables in vitro.
Sa composition présente une signature unique, propre à chaque individu, et résulte de la synthèse de la rencontre entre l’organisme hôte (ses gènes, son immunité) et son environnement (maladie, traitements, mode de vie, alimentation, mode de naissance, …).
Au plan fonctionnel, il est considéré aujourd’hui comme un organe à part entière. Parmi les fonctions portées par le microbiote et fortement impliquées dans le maintien de la santé de l’hôte, on peut décrire:
- Une fonction métabolique impliquée dans le métabolisme énergétique de l’hôte et le maintien de la barrière épithéliale intestinale avec la synthèse de dérivés métaboliques (vitamines, acides gras à chaînes courtes, dérivés du tryptophane, …) à partir des nutriments et substrats disponibles au niveau du colon.
- Une fonction endocrinienne portée par les métabolites microbiens qui vont exercer une action sur les circuits de régulations physiologiques comme celui de la glycémie, du système rénine-angiotensine-aldostérone, ou sur les systèmes nerveux central et entérique.
- Une fonction immunitaire avec un rôle dans le développement et la régulation du système immunitaire
- Une fonction de barrière vis-à-vis d’agents pathogènes.
C’est cette fonction barrière qui est particulièrement altérée dans le contexte de colite à Clostridioides difficile et que va permettre de restaurer la transplantation de microbiote fécal, seul traitement à l’heure actuelle permettant le transfert d’un éco-système intestinal complet.
«En quoi consiste la transplantation du microbiote fécale
Elle consiste à administrer chez un patient dont le microbiote est altéré, un microbiote issu d’un donneur sain en vue d’exercer des effets thérapeutiques.
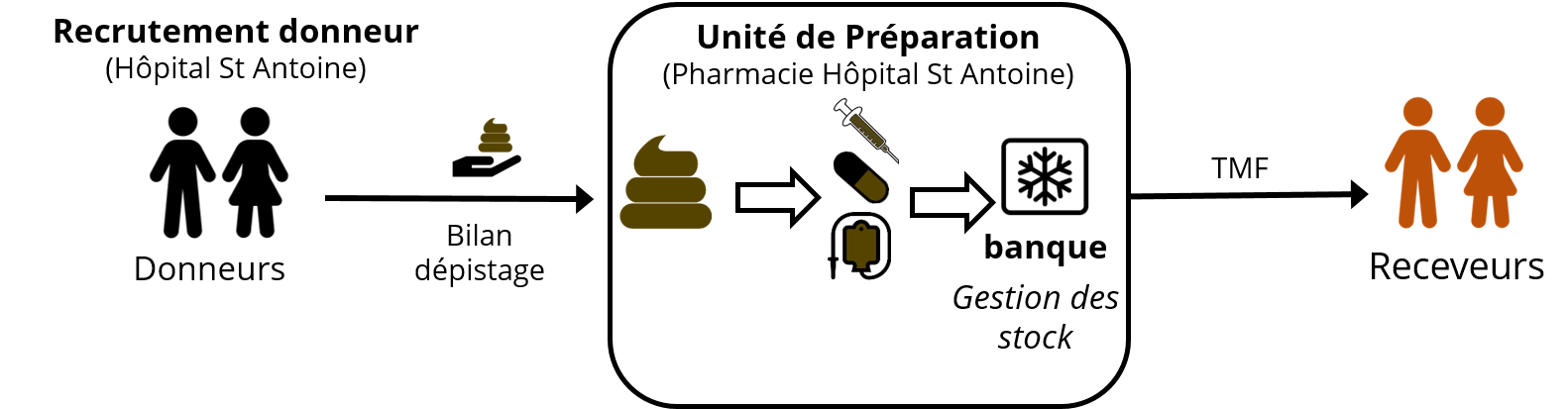 La TMF est actuellement le traitement le plus efficace pour traiter les infections récidivantes à Clostridioides difficile avec 80 à 90% d’efficacité. Elle est actuellement en cours d’évaluation dans le cadre de protocole de recherche dans plusieurs autres maladies.
La TMF est actuellement le traitement le plus efficace pour traiter les infections récidivantes à Clostridioides difficile avec 80 à 90% d’efficacité. Elle est actuellement en cours d’évaluation dans le cadre de protocole de recherche dans plusieurs autres maladies.
Description :
En pratique l’administration de la TMF se réalise en milieu hospitalier avec une surveillance médicale et paramédicale stricte. Dans le cadre du Centre, la TMF est réalisée soit sur le site de l’Hôpital Saint-Antoine (Hôpital de Jour ou hospitalisation conventionnelle dans le service de Gastro-entérologie et Nutrition), en infectiologie à la Pitié Salpetrière soit au sein d’un autre service hospitalier francilien.
La TMF est administrée par sonde naso-gastrique, gélule, coloscopie ou lavement en fonction de l’indication et des antécédents du patient. Une consultation de suivi est systématiquement organisée avec le médecin encadrant l’administration de la TMF à 10 semaines de la transplantation.
Dans le cadre du soin courant, le don est gratuit et anonyme. Les donneurs sont sélectionnés sur des critères cliniques stricts avec un bilan biologique et microbiologique permettant d’éliminer le risque d’une infection transmissible aux pathogènes connus selon les recommandations de l’ANSM.
Pourquoi donner ?
La transplantation de microbiote fécal est aujourd’hui considérée comme le traitement le plus efficace pour traiter les infections récidivantes par une bactérie appelée Clostridioides difficile. C’est aussi un traitement en cours d’évaluation dans plusieurs autres maladies comme les maladies inflammatoires chroniques de l’intestin (Maladie de Crohn et Rectocolite hémorragique) ou le syndrome de l’intestin irritable.
Cette thérapie innovante consiste à réintroduire chez le patient une flore bactérienne saine, prélevée dans les selles d’un donneur sain. Elle nécessite donc des dons et une structure pour les collecter, les caractériser, les préparer et les stocker.
Vous souhaitez devenir donneur ?
Répondez à ce questionnaire pour savoir si vous êtes éligible au don :
Vous pouvez aussi contacter :
Vous souhaitez plus d’information et échanger avec un professionnel de santé ? Vous pouvez écrire à donneurs.selles.sat@aphp.fr
Un.e infirmier.e vous contactera rapidement pour un entretien téléphonique pour savoir si vous êtes éligible.
Modalités du don de selles
Le don de selles est un acte sécurisé nécessitant une traçabilité : il n’est pas possible d’effectuer le recueil à domicile. Pour des raisons pratiques, il est donc recommandé d’habiter ou de travailler à proximité de l’hôpital Saint Antoine pour être donneur.
♦ Pour en savoir plus, cliquez ici
Le don de selles n’est pas rémunéré.
Titre long et court de l’étude: Essai randomisé prospectif multicentrique en double aveugle de transplantation de microbiote fécal (TMF) administrée par gélules versus placebo dans le syndrome de l’intestin irritable sévère (SII) – ICEBOAT (Ibs CapsulE microBiOtA Transplantation)
Promoteur: Assistance Publique-Hôpitaux de Paris
Centre coordinateur: Pr Jean-Marc SABATE – Service de Gastro-entérologie – Hôpital Avicenne 93000 Bobigny
Pathologie des patients: Le syndrome de l’intestin irritable (SII) est une maladie chronique caractérisée par des douleurs abdominales, des ballonnements et des troubles du transit (constipation, diarrhée ou alternance de diarrhée et de constipation), qui touche jusqu’à 10% de la population générale. L’efficacité des traitements disponibles est souvent limitée, en particulier dans le cas de formes sévères du SII qui concernent 20 à 25% des patients, et la maladie peut alors être responsable d’une altération importante de la qualité de vie.
La physiopathologie du SII est multifactorielle et différentes études ont suggéré un rôle du microbiote intestinal. Des études utilisant des techniques moléculaires ont montré des différences dans la composition du microbiote intestinal entre des patients avec SII et des sujets en bonne santé. Cette dysbiose pourrait jouer un rôle crucial car elle interagit avec l’alimentation et divers mécanismes impliqués dans le SII.
Objectif de l’essai : Évaluer l’efficacité de la TMF par rapport à un placebo sur le score de sévérité du SII à 12 semaines chez des patients présentant une forme sévère du syndrome de l’intestin irritable réfractaire aux traitements conventionnels.
Technique de transplantation: réalisée au moyen de gélules par voie orale contenant des selles congelées ou une solution de glycérol (placebo).
Numéro clinical trial de l’étude: NCT06433180
Mail de contact pour opposition à l’utilisation des selles dans l’étude: violonsel.urcest.drc@aphp.fr
Toute demande de transplantation de microbiote fécal doit être adressée par votre médecin à l’équipe du centre de transplantation fécale à l’adresse suivante : thuman.truong@aphp.fr
Titre long de l’étude : « Etude pilote d’une nouvelle technique de Transplantation Fécale Orale utilisant des gélules de selles congelées pour le traitement d’entretien des RCH à début pédiatrique. » T-FORE
Promoteur : Assistance Publique-Hôpitaux de Paris
Centre coordinateur : Dr Bénédicte PIGNEUR, Service de Gastro-entérologie et Nutrition Pédiatriques – Hôpital Necker-Enfants malades
Pathologie des patients : la Recto-Colite Hémorragique (RCH) en rémission chez l’enfant
Objectif de l’essai : Evaluer si la TMF par gélules de selles congelées chez les patients pédiatriques atteints de RCH, en rémission après traitement par corticoïdes, permet de modifier leur microbiote dysbiotique en augmentant la richesse de leur microbiote à 6 mois
Technique de transplantation : transplantation par gélules de selles congelées ou bien suspensions pour lavement intra-rectaux
Numéro clinical trial de l’étude : NCT05202990
Mail de contact pour opposition à l’utilisation des selles dans l’étude : crcest.violonsel.urcest.drc@aphp.fr



